
ELECTRICITE : 5°
1) Vrai ou faux
Dans un circuit fermé, l’interrupteur est ouvert.
Une ampoule est un générateur de courant.
2) Indiquez le symbole :
--> d’une ampoule :
--> d’une pile :
--> d’une DEL :
3) Quel est le rôle d’un récepteur dans un circuit?
4) On réalise le montage suivant.
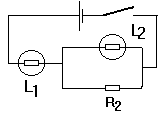
a) Indiquez le nom de tous les appareils dans ce schéma.
b) Les ampoules brillent-elles? Pourquoi?
c) Combien y a t-il de fils?
5)
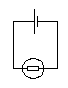
Voici le schéma d’un circuit électrique simple :
a) Citez les éléments qui le constituent.
b) Compléter le schéma avec les pôles de la pile et le sens du courant dans le circuit.
On peut améliorer un circuit en branchant un appareil qui permet de l’ouvrir ou de le fermer à volonté. Comment s’appelle t-il?
c) Refaire un autre schéma en y intercalant cet appareil (le circuit sera fermé).
Dans quel état se trouve alors la lampe?
6) Schématiser un montage série comprenant la résistance, une ampoule, un interrupteur et un générateur.
Placer en dérivation avec la résistance une deuxième ampoule
7) L’ampoule d’un phare d’une voiture est grillée. Le circuit de la voiture est-il en série ou avec dérivation? Justifier.
8) Une guirlande électrique de Noël comprend des lampes montées en série. Comment vérifier le montage.
9) Pour réaliser un montage électrique avec une pile plate, on assure les connexions avec des pinces crocodiles. Pourquoi faut-il prendre des précautions pour que les pinces ne se touchent pas?
10) Choisir la bonne réponse :
--> Le verre ne conduit pas le courant électrique : c’est un conducteur / isolant.
--> Le générateur / récepteur met en mouvement les électrons dans un circuit électrique fermé.
--> Le déplacement des électrons se fait de la borne positive / négative vers la borne positive / négative
11) Complétez le texte avec les mots suivants : fil - pile - bornes - électrique
Chaque appareil _______ possède toujours deux _________ . Elles peuvent être identiques ou différentes. Pour que l’appareil fonctionne, il faut que celles-ci soient réunies directement ou indirectement aux deux ______ d’une ______, directement ou indirectement par l’intermédiaire d’un _______.
12) En quel matériau est constitué le filament d’une ampoule?
13) Il existe deux types de culot d’ampoule : indiquez leur nom.
14) Quel est le nom du gaz en général contenu dans l’ampoule?
15)
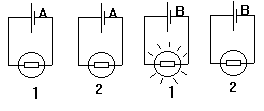
On a 2 piles A et B et 2 ampoules 1 et 2.
Indiquez si la pile A et B est usée et si les ampoules 1 et 2 sont bonnes.
ELECTRICITE : 4°
1) Quelle est l’unité de la tension? Quel est le symbole de l’unité?
Avec quel appareil mesure t-on la tension? Quel est son symbole électrique?
Comment se place t-il dans un circuit?
2) Réalisez un circuit série comprenant une pile, un interrupteur ouvert, une ampoule et une résistance. Placez le symbole du voltmètre pour mesurer la tension aux bornes de la résistance et un ampèremètre pour mesurer son intensité.
3) Réalisez un circuit série comprenant une pile, un interrupteur fermé, une ampoule. Placez une une diode en dérivation avec l’ampoule. Placez le symbole du voltmètre pour mesurer la tension aux bornes de la diode et un ampèremètre pour mesurer son intensité.
4)
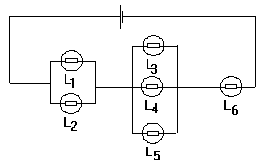
Le circuit ci-contre comprend 6 lampes. Aucune des lampes est identique sauf L3 , L4 et L5.
Indiquer l’intensité qui traverse chaque lampe sachant que : I6=1,6A et I2=1,1A
5) Compléter les phrases suivantes :
Dans un circuit série, l’intensité est ............................................ .
Dans un circuit série, la ................ des tensions aux bornes de chaque appareil est ................ à la tension aux bornes du générateur.
Dans un circuit dérivation, l’intensité débitée par la pile est ................... à la ......................... des intensités dans les branches ....................... .
Dans un circuit dérivation, la tensions aux bornes de chaque appareil est la................. .
6) Quelle est l’unité de la tension électrique? Indiquez son symbole. Avec quelle appareil mesure t-on la tension électrique? Comment se place t-il dans un circuit?
7) Quelle est l’unité de l’intensité du courant? Indiquez son symbole. Avec quelle appareil mesure t-on l’intensité du courant? Comment se place t-il dans un circuit?
8) Circuit série : il comprend un générateur et deux ampoules.
On appelle : U la tension aux bornes de la pile
U1 la tension aux bornes de l’ampoule L1
U2 la tension aux bornes de l’ampoule L2
On appelle : I l’intensité débitée par la pile
I1 l’intensité qui traverse l’ampoule L1
I2 l’intensité qui traverse l’ampoule L2
a) Refaites le schéma en plaçant l’ampèremètre pour mesurer I, puis un voltmètre pour mesurer U1.
d) Sachant que I=0,11A, indiquer la valeur de I1 et de I2.
Indiquez I en mA.
e) La tension aux bornes du générateur vaut 4,5V et celle aux bornes de L2 vaut 2,1V. Calculez la tension aux bornes de L1.
9) Un moteur et une ampoule sont placées en dérivation. Si la tension aux bornes du moteur est de 5V, quelle sera la tension aux bornes de l’ampoule? Expliquer.
10) Circuit série : le montage comporte une pile et deux ampoules
On appelle : U la tension aux bornes de la pile
U1 la tension aux bornes de l’ampoule L1
U2 la tension aux bornes de l’ampoule L2
On appelle : I l’intensité débitée par la pile
I1 l’intensité qui traverse l’ampoule L1
I2 l’intensité qui traverse l’ampoule L2
a) Faites le schéma en plaçant l’ampèremètre pour mesurer I1, puis un voltmètre pour mesurer U2.
b) Rappeler la définition d’un circuit série.
c) Compléter les phrases suivantes :
Dans un circuit série, l’intensité est ............................................ .
Dans un circuit série, la ................ des tensions aux bornes de chaque appareil est ................ à la tension aux bornes du générateur.
d) Sachant que I=0,31A, indiquer la valeur de I1 et de I2.
Indiquez I en mA.
e) La tension aux bornes du générateur vaut 6V et celle aux bornes de L2 vaut 2,1V. Calculez la tension aux bornes de L1.
11) Circuit dérivation : la diode est en dérivation avec l'ampoule
On appelle : U la tension aux bornes de la pile
U1 la tension aux bornes de la diode
U2 la tension aux bornes de l’ampoule
On appelle : I l’intensité débitée par la pile
I1 l’intensité qui traverse la diode
I2 l’intensité qui traverse l’ampoule
a) Faites le schéma en plaçant l’ampèremètre pour mesurer I1, puis un voltmètre pour mesurer U2.
b) La diode est-elle correctement placée? Quel est son rôle?
c) Compléter les phrases suivantes :
Dans un circuit dérivation, l’intensité débitée par la pile est ................... à la ......................... des intensités dans les branches ....................... .
Dans un circuit dérivation, la tensions aux bornes de chaque appareil est la................. .
d) Sachant que I1=0,42A et I=0,74A, calculez la valeur de I2.
Indiquez I en mA.
e) La tension aux bornes du générateur vaut 6V. Indiquez la tension aux bornes de la diode et de l’ampoule.
12) Lampe grillée
Une guirlande électrique comprend cinq lampes portant les indications suivantes : 1,2V ; 0,22A montées en série.
a) Faites le schéma électrique du circuit.
b) Quelle doit être la tension aux bornes du générateur pour que les lampes fonctionnent normalement.
c) Une lampe grille. Que se passe t-il?
d) Eric affirme pouvoir trouver la lampe grillée avec un voltmètre? Pourquoi?
13) Pourquoi parle t-on d'intensité pour le courant électrique ?
Quelle est l'unité de l'intensité du courant électrique ? Et son symbole ?
Avec quel appareil mesure t-on cette intensité? Quel est son symbole ?
Que signifie le mot " calibre " ? Par quoi lequel doit-on commencer ? Et ensuite, que fait-on ? Pourquoi ?
14)
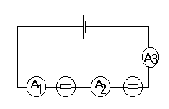
Voici un circuit en série. Plusieurs mesures d'intensité sont réalisées.
a) Qu'observe t-on?
b) Quelle conclusion peut-on en tirer?
15) Exprimer dans l'unité demandée :
450A= kA
0,25A= mA
0,45mA= µA
1,24µA= nA
16) Montages série et dérivation
Réaliser le schéma d'un montage série comprenant la résistance R2, une ampoule, un interrupteur ouvert et un générateur.
Réaliser le schéma un montage série comprenant la résistance R2, un interrupteur fermé, un moteur et un générateur. Placer une ampoule en dérivation avec la résistance R2 et une diode en dérivation avec le moteur.
17) Montage plus complexe
Réaliser le schéma un montage série comprenant la résistance R2, une ampoule, un interrupteur ouvert et un générateur. Placer en dérivation avec la résistance R2 une deuxième ampoule, puis en dérivation avec la première une del. Enfin, placez en dérivation avec cette del un moteur.
18) Discussion entre 2 élèves
- Au fait, tu as compris le cours de Physique sur les générateurs.
- Oui, pourquoi ?
- Moi, je ne sais pas ce qu'est un générateur !
- C'est simple, ………………………………………………………………………….
- Ah ! Oui, mais alors quel est le rapport entre le générateur et les ouvriers pousseurs ?
- …………………………………………………………………….
- D'accord ! Les ouvriers poussent les wagons comme……………………………………
Et alors, pourquoi l'ampoule brille t-elle ?
- Décidément, tu n'écoutes rien ! C'est………………………………………….
- Mais pourquoi parle t-on d'intensité du courant ?
- ………………………………………………………………………………..
- Et on la mesure avec un ampère !
- Mais non ! C'est un ………………….. . L'ampère, c'est …………………………………..
- Et bien, jamais j'y arriverais !
- Mais si, il te suffit d'apprendre un peu !
Complétez les phrases.
19) Nouvelle discussion
- On fait un TP aujourd'hui ?
- Oui, c'est chouette. Tu as révisé un peu ?
- Oui, mais je ne sais pas si je peux faire les mesures !
- Pourquoi ?
- Je sais qu'il faut le placer en dérivation, et ce n'est pas facile !
- Oui, et on commence toujours par le calibre le plus petit, 200mA, tout ça pour une meilleure précision !
- C'est simple, le plus étant le COM, et on y va !
- Tiens, j'ai un nombre négatif !
- C'est normal, mais tu es vraiment nul !
- Donc, cela fait -134,2.
- -134,2 quoi ?
- Ce sont des ampères !
- Tu es sûr ?
- Oui, oui, pourquoi ?
- Le chiffre me paraît énorme, pas toi ?
- Non.
Que d'erreurs dans ces manipulations, réécrivez cette discussion en indiquant le déroulement correct !
21)
Donnez la définition des mots suivants : isolant, conducteur, montage en série ,
montage en dérivation, court-circuit.
22)
Schématiser un montage série comprenant la diode, une ampoule, un interrupteur
ouvert et un générateur.
Placer en dérivation avec lampoule une DEL.
23) Schématiser un montage série comprenant un moteur, une ampoule, un interrupteur fermé et un générateur.
Placer
en dérivation avec le moteur une deuxième ampoule.
ELECTRICITE : 3°
1) Recopiez et compléter
--> L’unité d’intensité I du courant électrique est ...............; son symbole est .................. .
--> La tension aux bornes d’un dipôle se mesure avec un ......................; cet appareil se branche en ............................. .
--> L’ampèremètre se branche en ....................... dans le circuit.
2)
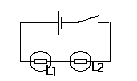
Dans ces 2 montages, on appelle :
--> U la tension aux bornes du générateur, I l’intensité du courant qui traverse.
--> U1 et U2 les tensions aux bornes de L1 et L2 , I1 et I2 les intensités qui les traversent.
Indiquer les relations que l’on peut appliquer pour chacun ce montage.
/4,5 3) On considère le circuit suivant :
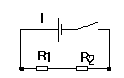
La tension aux bornes du générateur vaut 6V et celle aux bornes de R1 est 3,5V.
On mesure I : on trouve I=565mA.
a) Refaire le schéma en plaçant un ampèremètre pour mesurer I et un voltmètre pour mesurer la tension aux bornes de R1 (indiquer la borne + et le COM).
Indiquer le sens du courant sur le schéma et rappeler le sens des électrons.
b) Comment R1 et R2 sont-ils placées (en série ou dérivation)? Déduire la tension aux bornes de R2.
c) Indiquer l’intensité dans le générateur et dans les 2 résistances (expliquer vos résultats).
4) Choisissez le calibre
On veut mesurer la tension aux bornes d’une pile (la tension indiquée sur la pile est de 9V). Les calibres indiqués sur le voltmètre sont : 200mV, 2V, 20V, 200V.
a) Rappeler la définition du mot calibre.
b) La pile est neuve. Quel calibre doit-on choisir de préférence? Pourquoi?
c) Quels autres calibres peut-on utiliser?
5) On dispose d’une pile, de trois lampes identiques, d’un interrupteur et d’un moteur.
a) Réaliser un montage série comportant tous les composants.
b) La tension aux bornes du moteur est de 3V, et celle aux bornes de chaque lampe est de 1,5V. Calculez la tension aux bornes du générateur.
c) Une lampe est grillée, les autres brillent-elles? Quelle est alors la tension aux bornes de chacune d’elles?
6) Exprimer dans l’unité demandée (écriture scientifique) :
430V= kV
0,2V= mV
15mV= kV
12400µV= V
7) On dispose d’une pile, de trois lampes identiques, d’un interrupteur et d’un moteur.
a) Réaliser un montage série comportant tous les composants.
b) La tension aux bornes du moteur est de 3V, et celle aux bornes de chaque lampe est de 1,5V. Calculez la tension aux bornes du générateur.
c) Une lampe est grillée, les autres brillent-elles? Quelle est alors la tension aux bornes de chacune d’elles?
8) Rappeler la définition d’une tension continue et d’une alternative.
9) Donnez la définition de la période, de la fréquence, de la tension maximale et de la tension efficace.
N’oubliez pas les unités.
10) Oscilloscope : quel est son rôle? Combien a t-il de bornes?
11) a) En France, la période du secteur est de 0,02s. Calculer la fréquence correspondante.
b) Aux Etats-Unis, la fréquence vaut 60 Hz. Calculez la période correspondante.
12) Comment obtenir une tension alternative.
13) Représentez l’écran d’un oscilloscope avec balayage déclenché lorsqu’à ses bornes :
a) aucune tension n’est appliquée
b) une pile est branchée
c) le générateur du collège est branché sur la position « alternatif »
14) Rappeler la définition de la puissance consommée et de l’énergie électrique consommée. N’oubliez pas les unités.
15) La recette du pain d’épice
- 350g de miel
- 250 g de farine
- 1 verre de lait tiède
- 1 cuillère à café d’hydrogénocarbonate de sodium (encore appelé bicarbonate de soude)
Verser le mélange dans un moule à cake préalablement beurré.
Préchauffer le four (thermostat 4) puis enfourner et laisser cuire environ 1 h.
Chez les Dupont, la cuisson du pain d’épice dure 55min. Le four électrique réglé sur le thermostat 4 consomme une puissance moyenne de 650W.
Chez les Dupond, la pain d’épice est moelleux au bout de 1 h 5 min; leur four consomme une puissance de 620W.
Calculez l’énergie consommée dans chaque famille pour faire cuire le pain d’épice, ainsi que le prix de revient (le kWh coûte 0,75F).
16) Sur le culot d’une lampe, on peut lire : 12V; 21W.
Calculez l’intensité du courant I qui traverse cette lampe en fonctionnement normal.
17) Calculez en kWh les énergies consommées par les différents appareils du tableau :
appareil magnétoscope radio-réveil téléviseur
puissance 20W 4W 65W
durée de fonctionnement 3 h 30 min 24 h 2h 40 min
18) Recopiez et compléter :
L’énergie électrique reçue par un appareil se mesure en ......., de symbole ......... ou en .............. de symbole ........... .
La puissance électrique reçue par un appareil se mesure en ............. de symbole .............. .
Circuit dérivation
19) La diode est en dérivation avec l'ampoule.
On appelle : U la tension aux bornes de la pile
U1 la tension aux bornes de la diode
U2 la tension aux bornes de l’ampoule
On appelle : I l’intensité débitée par la pile
I1 l’intensité qui traverse la diode
I2 l’intensité qui traverse l’ampoule
a) Refaites le schéma en plaçant l’ampèremètre pour mesurer I1, puis un voltmètre pour mesurer U2.
b) Recopiez et compléter les phrases suivantes :
Dans un circuit dérivation, l’intensité débitée par la pile est ................... à la ......................... des intensités dans les branches ....................... .
Dans un circuit dérivation, la tensions aux bornes de chaque appareil est la................. .
c) Sachant que I1=0,42A et I=0,74A, calculez la valeur de I2.
Indiquez I en mA.
d) La tension aux bornes du générateur vaut 6V. Indiquez la tension aux bornes de la diode et de l’ampoule.
20)
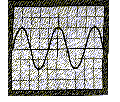
Sur l'écran d'un oscilloscope, on observe la tension entre les bornes d'un alternateur.
Sachant que la sensibilité verticale de l'oscilloscope est 2 V par cm et la durée de balayage 2,5ms par cm, calculez :
a) la tension maximale, puis la tension efficace.
b) la période et la fréquence de la tension alternative.
Indiquez tous les calculs.
21)
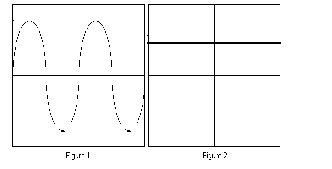
Les schémas ci-dessous représentent des figures observées sur l'écran d'un oscilloscope. Indiquez quelle est la tension continue et la tension alternative.
Rappeler la définition d'une tension continue et d'une alternative.
22) Choisir le calibre dun ampèremètre
Un multimètre utilisé en ampèremètre possède les calibres suivants : 2A, 200mA, 20mA, 2000µA.
On la placé en un point du circuit où lintensité est de 165mA
a) Quels calibres peuvent être utilisés sans risquer de détériorer lappareil ?
b) Parmi ces calibres, quel est le meilleur calibre utilisable ?
23) Dans le circuit, les lampes L1 et L2 ne sont pas identiques. L1 est traversée par un courant dintensité 30 mA. Peut-on savoir lintensité indiquée par lampèremètre A2 ? Si oui, indiquer cette valeur et justifier la réponse.
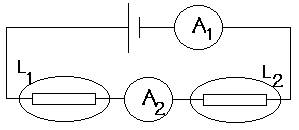
24) Le voltmètre V1 indique une tension de 8,5V.
Quindique le voltmètre V2 ? Justifier votre réponse.
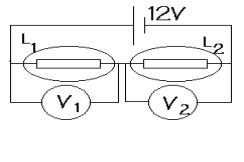
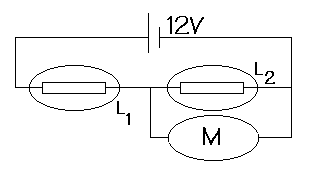
25) Le moteur et la lampe L2 sont placés en série ou en dérivation ?
a) La tension aux bornes du moteur vaut 4,5V, quelle est celle aux bornes de L2 ?
b) Déduire alors celle aux bornes de L1 ?
c) Lintensité du courant débitée par le générateur vaut 360mA, convertissez en A.
d) Indiquer lintensité aux bornes de tous les composants sachant que lintensité qui traverse le moteur vaut 130mA.
e) Sur le culot de lampoule L1, il y a marqué 6V et 0,3A. Brillera t-elle normalement ?
CHIMIE : 5°
1) Vrai ou faux
L’eau se vaporise uniquement à 100°C
La glace, c’est de l’eau
La température s’exprime en degré centigrade
Toutes les températures sont positives
2) Représentation graphique
On réalise la fusion du naphtalène. On relève la température toutes les minutes :
Temps (min) 0 1 2 3 4 5 6 7 8 9
Température (°C) 20 28 37 46 56 65 74 77 77 78
Temps (min) 10 11 12 13 14 15 16
Température (°C) 78 78 79 82 83 93 99
Faire une représentation graphique de l’expérience.
Est-ce un corps pur? Pourquoi?
3) Que se passe t-il si on place une bouteille remplie d’eau et bouché au congélateur?
Quelles précautions faut-il prendre l’hiver avec les canalisations contenant de l’eau, un bassin,... ?
4) Lis les phrases suivantes et écris dans chaque case :
E pour Evaporation ; C pour Condensation ; S pour Solidification et F pour Fusion
Les jours de vent, le linge sèche vite
Les jours de grand froid, les flaques d’eau gèlent
Quand les vitres se couvrent de buée, on peut dessiner dessus
En hiver, le givre se forme sur les vitres de la voiture
L’eau d’un torrent provient d’un glacier
5) On a 175g de glaçons. On les laisse fondre. Quelle masse d’eau liquide obtient-on?
Que peut-on dire du volume?
6) Rappel de math : prendre 65% de A, c’est multiplier 65 % de A et diviser par 100.
Un homme pèse 70kg. Il est constitué de 65% d’eau. Calculer la quantité d’eau qu’il contient.
7) Mélange et corps pur
Les catalogues de produits chimiques indiquent souvent les températures de fusion ou d’ébullition de certains produits.
Comment reconnaît-on un corps pur d’un corps non pur?
Dans la liste ci-dessous, entourer le nom des corps purs :
éther de pétrole (teb : 40 à 60 °C)
paraffine (tf : 52 à 54 °C)
anthracène (tf : 216°C)
trichloréthylène (teb : 87°C)
kérosène (teb : 150 à 300°C)
zinc (tf : 419,5°C)
8) Indiquer la température de fusion et de vaporisation de l’eau pure.
9) Avec quels appareils mesure t-on la température et la pression atmosphérique?
10) Indiquez la masse d’un litre d’eau.
On a un bêcher qui contient 2,73cL d’eau. Quelle est la masse de l’eau en cg, puis en g.
11) Convertissez :
10,3g =.............. mg 20L =.......... mL 10,2dL =......... mL
0,51kg =................. g 0,1cL =......... mL 50cL =............ L
1,50kg =.............mg 1,8mL =............ L 110mL =.......... L
12) Un chimiste veut mesurer 200 mL d’eau.
Quel récipient va t-il utiliser? Faites un schéma.
Il veut peser cette eau. Comment fera t-il? Faites un schéma.
Quelle masse va t-il trouver en mg, puis en g.
13) Une salière en verre contenant du sel fin tombe et se casse. Imaginez et schématisez une méthode permettant de récupérer le sel. La méthode est-elle valable pour du sucre?
14)
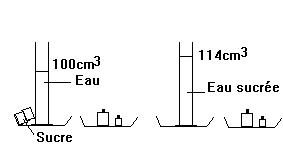
On réalise l’expérience décrite à gauche
Déduisez 2 conclusions.
Peut-on obtenir un litre d’eau sucrée (à 100g/L) en dissolvant 100g de sucre dans un litre d’eau?
15) Indiquez la carte d’identité de l’eau
16) Qu’est-ce qu’une molécule?
17) Comment peut-on obtenir une solution d’eau sucrée de concentration 100g/L. Faites des schémas.
Comment pourrait-on réobtenir ensuite cette eau?
18) Vrai ou faux
Le jus de fruit est constitué d’eau
Les constituants d’un mélange homogène ne peuvent être séparés
Un filtre ne laisse passer que l’eau
19) La vinaigrette
a) Comment obtient-on la vinaigrette?
b) Dans quelle catégorie de mélange peut-on la classer?
c) Peut-on séparer facilement les constituants?
20) Pourquoi est-il nécessaire d’agiter certaines boissons à base de jus de fruit avant de les consommer?
Que donnerait la centrifugation d’un jus de fruit?
Pourquoi les fabricants de jus d’orange laissent-ils parfois une partie du fruit?
21) Indiquer le nom des 4 méthodes de séparation. Faites les schémas pour la filtration et la distillation.
22) a) Souffler dans de l’eau de chaux y produit un trouble blanc. Que contient l’air expiré?
b) Une soucoupe contenant de l’eau de chaux est laissée à l’air libre. Après quelques heures, elle se recouvre d’un voile blanc. Que peut-on conclure?
c) Pourquoi doit-on conserver l’eau de chaux dans des bouteilles hermétiquement closes?
Pourquoi utilise t-on le plus souvent de l’eau de chaux fraîchement préparée?
23) Certains comprimés mis dans l’eau produisent une effervescence. Une allumette placée juste au dessus s’éteint. Le gaz prélevé avec une seringue trouble l ’eau de chaux. Que contiennent les bulles?
24) Pourquoi est-il préférable d’ouvrir une boisson gazeuse après l’avoir refroidie suffisamment et en évitant de l’agiter?
Que se passe t-il si on ne respecte pas l’une de ces précautions?
25) Robert est curieux. Il désire connaître le gaz qui est dissous dans une bouteille de champagne.
a) Indiquez la méthode pour recueillir un gaz. Faites un schéma.
b) Le gaz, étant recueillit dans un tube à essai, Robert ajoute un réactif particulier. Quel est ce réactif? Que va t-il se passer quand il sera dans le tube contenant le gaz?
c) Quel gaz vient-on de caractériser? Robert peut donc conclure sur le gaz contenu dans le champagne.
26) Rappeler la carte d’identité du dioxyde de carbone.
27) Qu’est ce que l’effet de serre?
28) Comment mesure t-on le pH?
Le pH est compris entre quel chiffre?
Comment appelle t-on les solutions qui ont un pH supérieur à 7, égal à 7 et inférieur à 7?
29) Comment s’appelle le lieu où on traite les eaux?
30) RECHERCHE SUR LA CONSOMMATION DOMESTIQUE D’EAU
Calcul du prix TTC (Toutes Taxes Comprises) du m3 d’eau dans une ville
Rechercher les factures d’eau les plus récentes sur un an (il y en a en principe une toutes les 6 mois)
Rechercher la consommation totale en m3 pour un an................ m3 d’eau par an
Rechercher le prix total de l’eau pour un an................ F par an
Ecrire la phrase suivante avec les valeurs trouvées
......... m3 d’eau dans la ville ................. coûtent ..........F
En déduire le prix du m3 d’eau dans la ville
1 m3 d’eau dans la ville ................. coûte ............F
Comparer le prix trouvé avec celui des autres communes environnantes
Calcul de la consommation individuelle journalière (ou combien d’eau consomme t-on chaque jour?)
Reprendre la consommation totale annuelle pour toute la maison
................ m3 d’eau par an pour .......... personnes
Calculer la consommation individuelle par personne et par an................ m3 d’eau par personne et par an
Convertir les m3 en litres pour plus de commodité (1 m3 = 1000 L)
................ m3 = ............ L
Calculer la consommation individuelle par personne pour un jour en litres
Chaque personne consomme ........... L d’eau par jour
31) La masse d’un atome de carbone est d’environ 2.10-23 g.
Quel le nombre d’atomes de carbone présent dans 1 g de carbone?
32) Trois flacons, alignés sur une table, contiennent chacun un gaz différent : air, dioxygène et dioxyde de carbone.
a) Est-il possible d’identifier chacun de ces gaz grâce à une observation des flacons? Justifier votre réponse.
b) Quel est le test unique qui peut permettre d’identifier chacun de ces gaz?
33) Robert est curieux. Il désire connaître le gaz qui est dissous dans une bouteille de champagne.
a) Indiquez la méthode pour recueillir un gaz. Faites un schéma.
b) Le gaz, étant recueillit dans un tube à essai, Robert ajoute un réactif particulier. Quel est ce réactif? Que va t-il se passer quand il sera dans le tube contenant le gaz?
c) Quel gaz vient-on de caractériser? Robert peut donc conclure sur le gaz contenu dans le champagne.
34) On décompose de l’eau dans une cuve à électrolyse.
a) Quel sont les deux gaz qui apparaissent? Quel gaz apparaît en plus grande quantité?
b) Rappeler comment les caractériser?
35) Rappeler la carte d’identité du dioxyde de carbone.
36) Qu’est ce que l’effet de serre?
37) Avec quels appareils mesure t-on la température?
Indiquer la température de fusion et de vaporisation de l’eau pure.
38) Comment peut-on faire pour caractériser de l'eau (citez deux exemples)? Faire un schéma des expériences.
39) Comment reconnaît-on un corps pur d'un corps non pur?
40) Un volume V=100cm3 de cyclohexane a une masse M=78g.
a) Schématiser la suite des manipulations à faire pour obtenir ces résultats.
b) En déduire la masse d’un litre de cyclohexane.
CHIMIE : 4°
1) Rappelez la définition d’un atome et d’une molécule.
2) Indiquer le nombre de chaque atome dans les molécules suivantes : H2O, H2, CO2, CO, O2.
N’oubliez pas de préciser leur nom.
3) Indiquez la formule des molécules suivantes :
hexane : elle est composée de 6 atomes de carbone et 14 atomes d’hydrogène.
trioxyde de soufre : elle est composée d’un atome de soufre (symbole S) et de 3 atomes d’oxygène.
4) Trois flacons, alignés sur une table, contiennent chacun un gaz différent : dihydrogène, dioxygène et dioxyde de carbone.
a) Est-il possible d’identifier chacun de ces gaz grâce à une observation des flacons? Justifier votre réponse.
b) Quel est le test unique qui peut permettre d’identifier chacun de ces gaz?
5) Composition de l’air
a) Quelle est la composition des principaux gaz constituant l’air?
b) Quel est le volume de dioxygène présent dans 10L d’air?
c) Quel est le volume de diazote présent dans 10L d’air?
6) Mickael pèse son ballon de basket. Il trouve une ma sse de 935,4g. Il le dégonfle un et recueille 4,5L d’air. Il pèse à nouveau son ballon et trouve une masse de 929,6g.
Quelle est la masse d’un litre d’air?
7) Quelle propriété de l’air permet d’emmagasiner une grande quantité d’air dans les bouteilles d’un plongeur?
8) Mission Apollo
Le 21 juillet 1969, l’astronaute américain Edwin Aldrin est photographié par Neil Amstrong sur la surface de la Lune.
a) Explique pourquoi il est enfermé dans un scaphandre étanche.
b) Quels sont, à ton avis, les équipements de survie qui lui ont été nécessaires pour pouvoir se déplacer sur le sol lunaire?
9) Des bulles dans l ’aquarium
a) Dessine quelques bulles qui montent du fond d’un aquarium en respectant leurs dimensions.
b) Pourquoi aère t-on en permanence l’eau dans laquelle vivent les poissons?
10) Quelle est la composition de l’air qui nous entoure (n’oubliez pas les pourcentages)?
Quel est le nom du chimiste qui l’a découvert?
11) Le dioxygène est-il présent sur toutes les planètes du système solaire?
12) Combien pèse 1L dair? Et 2L? Et 0,5L?
13) Le volume de l’air varie t-il? Comment dit-on lorsqu’il augmente, lorsqu’il diminue?
14) Citez quelques exemples de gaz polluants? Citez des exemples de corps polluants?
15) La composition de l’air inspiré et de l’air expiré est-il la même (dire lesquelles et pourquoi)?
16) Qui n’a pas oublié son repas sur le « feu »? Laissé trop longtemps à la chaleur, le beurre brunit puis noircit et l’on peut observer au fond de la poêle des petites particules de carbone. Il s’est également formé de la vapeur d’eau.
Rappelez le sens de l’expression « changement d’état ». Citez le nom des 6 changements d’état.
Le beurre subit-il un changement d’état? une réaction chimique? Justifiez votre réponse.
17) Nous inspirons du dioxygène et expirons du dioxyde
de carbone. Pendant la journée, les plantes prélèvent plus de dioxyde de carbone dans l’atmosphère qu’elles n’en rejettent. Grâce à la chlorophylle, le dioxyde de carbone et l’eau se combinent pour former du glucose et libérer du dioxygène : c’est la photosynthèse.
a) La photosynthèse est-elle une réaction chimique. Justifiez votre réponse.
b) Si oui, quels sont les réactifs, les produits et écrire le bilan.
18) Que signifie les mots combustion, comburant et combustible?
19) Quel est le gaz obtenu lors de la combustion complète et incomplète du carbone?
20) Que signifie les mots réactifs et produits?
21) Est-il prudent de boucher les aérations dans une maison? Citez deux raisons.
21) Vrai ou faux
- Le monoxyde de carbone possède une odeur désagréable
- Un changement d’état est une réaction chimique
- Le monoxyde de carbone est dangereux
- Le fusain est du dioxyde de carbone
- En cas de fuite de gaz, il ne faut pas utiliser le courant électrique.
- L’eau de chaux permet de caractériser la présence d’eau
22) Chaque été se produit des feux de forêt. Rédige trois recommandations pour les promeneurs et automobilistes en forêt.
23) Le lait contient des ions calcium en quantité importante (125mg pour 100mL).
Calculer sa concentration massique.
24) Indiquer le symbole des atomes d’hydrogène, de carbone et d’oxygène.
25) Rappelez la définition d’une molécule.
26) Indiquer le nombre d’atomes dans les molécules suivantes : H2O,H2, CO2, CO, O2.
27) Indiquez la formule des molécules suivantes :
--> hexane : elle est composée de 6 atomes de carbone et 14 atomes d’hydrogène.
--> trioxyde de soufre : elle est composée d’un atome de soufre (symbole S) et de 3 atomes d’oxygène.
--> glucose : elle est composée de 6 atomes de carbone, de 12 atomes d’hydrogène et 6 atomes d’oxygène.
28) Comment reconnaît-on qu’il y a une réaction chimique (citez au moins trois exemples)?
29) Le carbone et le dioxygène réagissent pour former du dioxyde de carbone. Ecrire l’équation-bilan.
30) Le carbone et le dioxygène réagissent pour former du monoxyde de carbone. Ecrire l’équation-bilan et pensez à l’équilibrer.
31) Triangle du feu
Pourquoi
la plupart des incendies d'habitation naissent-ils dans les cuisines ?
Faites
le triangle du feu.
Comment
doit-on procéder si l'on veut arrêter un incendie.
32)
Pourquoi les jours de mistral sont-ils classés à haut risque pour les forêts
méditerranéennes ?
33)
Pourquoi est-il conseillé de :
--
souffler sur les braises d'un barbecue si on veut activer le feu ?
--
fermer les portes et les fenêtres avant d'évacuer la salle de classe en cas
d'alerte à l'incendie ?
--
envelopper dans une couverture une personne dont les vêtements sont en feu ?
34)
La combustion du propane dans une chaudière à gaz produit du dioxyde de
carbone et de leau.
La
combustion est-elle incomplète ou complète ? Justifier
35)
Recopiez et choisissez la bonne réponse :
Une
combustion complète / incomplète produit du dioxyde de carbone.
Le
dioxyde de carbone est / n'est pas toxique.
Respirer
un air riche en dioxyde de carbone présente / ne présente pas des
risque d'asphyxie.
Le
monoxyde de carbone est un gaz coloré / incolore, inodore / odorant, peu / très toxique.
36)
Qu'est-ce qu'un atome ? Qu'est-ce qu'une molécule ?
37)
Trouver la formule des molécules suivantes à partir des atomes qui les
constituent :
La
molécule de butane formée de 4 atomes de carbone et dix atomes d'hydrogène.
La
molécule deau oxygénée formée de deux atomes d'hydrogène et de deux
atomes d'oxygène.
La
molécule de glucose formée de 6 atomes de carbone, 12 atomes d'hydrogène, et
6 atomes d'oxygène.
38)
Recopiez et compléter le tableau suivant :
|
NOM |
COMPOSITION |
FORMULE |
MODELE MOLECULAIRE |
|
Dioxygène |
|
|
|
|
Eau |
|
|
|
|
Dioxyde de carbone |
|
|
|
39)
Recopiez et compléter le tableau suivant :
|
|
REACTIFS |
PRODUITS |
|
COMBUSTION DU CARBONE |
|
|
|
COMBUSTION DU BUTANE |
|
|
|
COMBUSTION DU FER |
|
|
40)
Indiquez le nombre de chaque atomes dans les molécules suivantes : C3H8,
C2H6O, H2O2, NO2.
41)
Indiquez la formule des composés suivants :
Diazote
: 2 atomes dazote
DDT
: 14 atomes de carbone, 9 atomes dhydrogène et 4 de chlore
Acide
sulfurique : 2 atomes dhydrogène,
1 atome de soufre et 4 atomes doxygène.
CHIMIE : 3°
1) Recopiez et complétez :
L’action du dioxygène de l’air sur les métaux est une ...........
Les produits de la réaction sont des corps purs composés appelés .......................
2) Rappeler la définition d’un atome, d’une molécule, d’un corps simple et d’un corps composé.
3) Indiquer le nombre d’atomes dans chacune des molécules :
C4H9O : C5H12 :
H2O2: CO2 :
4) Faites correspondre le métal à son produit de corrosion :
Métal : aluminium, fer, cuivre.
Oxyde métallique : vert de gris, alumine, rouille.
5) L’acier inoxydable 18/10 contient , en masse, 18% de chrome et 10% de nickel. Calculez les masses de chrome, de nickel et de fer dans 500kg de cet acier.
6) Dans un cristal d’oxyde de fer, il y a 150 atomes d’oxygène pour 100 atomes de fer.
Sa formule est-elle : FeO, Fe2O3, Fe3O4?
7) Equilibrez les réactions suivantes :
Al + O2 --> Al2O3
Fe + O2 -->Fe3O4
8) Le cuivre réagit dans l’air avec le dioxygène pour former un oxyde de cuivre CuO.
a) Ecrivez l’équation-bilan (pensez à l’équilibrer)
b) Quelques fois, il se forme un oxyde de cuivre II Cu2O. Ecrivez la nouvelle équation-bilan.
c) Il peut se former les deux produits en même temps. Ecrivez la nouvelle équation-bilan.
9) Indiquer le nombre d’atomes dans chacune des molécules :
C4H9O : C3H8 :
H2O2: CO2 :
CO : O3 :
10) Equilibrez les réactions suivantes : (Hg est le symbole de l’atome de mercure)
Al + O2 -->Al2O3
Hg + O2 -->HgO
11) Ecrivez l’équation-bilan de l’oxydation du chrome de symbole Cr, sachant qu’il se forme l’oxyde de chrome de formule Cr2O3.
12) Quel est la protection qu’offre l’oxyde de cuivre et que n’offre pas la rouille? Est-ce un avantage?
13) Une histoire de casserole
Parmi les métaux usuels envisagés (cuivre, fer, aluminium et zinc) :
a) Quels sont ceux qui ne sont pas utilisés pour faire des casseroles?
b) Quels sont les avantages et les inconvénients de l’aluminium dans la réalisation de casserole?
c) Pourquoi les casseroles en cuivre sont-elles étamées intérieurement?
d) Quels sont les nouveaux matériaux utilisés dans la fabrication de casseroles? Justifier votre choix.
14) Le chauffage d’un morceau de fer dans un four à 900°C provoque la formation d’un oxyde métallique.
a) Qu’est-ce qu’une oxydation?
b) La masse de fer croît-elle?
c) La température de fusion du fer est de 1535°C. Rappeler la définition de la fusion.
d) Le fer fond t-il avant de s’oxyder?
c) Le fer s’oxyde t-il lorsque le forgeron le chauffe dans le foyer?
15) Corrosion et pollution
a) Que signifie le terme corrosion?
b) Tous les métaux ont-ils le même comportement au contact de l’air atmosphérique?
16) Quelles sont les atomes qui constituent en majorité les matériaux organiques et les verres?
17) Quels sont les dangers de la combustion des matériaux organiques?
18) Quels sont les produits formés lors de la combustion des matériaux organiques (par exemple le papier)? Comment pourrait-on prouver leur présence? Faire des schémas des expériences possibles.
19) Recopiez et complétez :
Une solution qui a un pH de 4 est une solution dite ............ , par exemple, comme ............... ....................... . Par contre, une solution qui a un pH supérieur à 7 est une solution dite ............. , comme la .............. .
20) Un chimiste désire ranger des produits chimiques. Il a trois tubes à essai de solutions qui sont de couleurs différentes : le tube 1 a une couleur bleue, le 2 et le 3 sont incolores. Pour savoir ce qu'ils contiennent, il ajoute un peu de soude.
Dans le premier, il voit apparaître un précipité bleu, dans le deuxième et le troisième un précipité blanc.
a) Que contiennent les tubes à essai 1,2 et 3?
b) Dans les tubes 2 et 3, il ajoute un excès de soude. Pourquoi? Le précipité disparaît dans le tube 2 et non pas dans le tube 3. Que peut-on conclure?
21) Dans un tube à essai, on met du zinc. On ajoute un peu d'acide chlorhydrique.
a) Y a-t-il réaction chimique? Pourquoi?
b) Expliquez ce que l'on peut faire pour caractériser les produits formés.
c) Ecrire l'équation-bilan de la réaction chimique.
22) Dans un bêcher, Brigitte ne sait plus si elle a mis une solution d'acide chlorhydrique ou de soude. Elle en verse un peu dans un tube à essai contenant du chlorure de fer II . Il n'y a pas apparition d'un précipité. Quelle est la nature de la solution dans le bêcher?
23) 80kg de bois donnent autant de chaleur que 47 kg de charbon de bonne qualité.
Calculez la quantité de bois équivalente à 100kg de charbon.
24) A chacun son test : indiquer par une croix, les réactifs permettant d’identifier les espèces chimiques notées dans le tableau.
Al3+ Zn2+ Fe2+ CO2
Soude
eau de chaux
acide chlorhydrique
25) Pluies acides :
a) Citer une conséquence des pluies acides sur les bâtiments ayant des matériaux calcaires.
b) Citer une conséquence des pluies acides sur les constructions métalliques en fer.
26) a) Parmi les liquides ci-dessous, nommer ceux qui sont acides. Justifier la réponse. Boisson au cola : 2,5; jus de citron : 3; cidre : 3,5; bière : 4; lait : 6,6; eau minérale : 7,2; eau de chaux : 10; eau de Javel : 12.
b) Parmi ces liquides, quel est celui qui a la plus grande concentration en ions hydrogène?
c) Comment sont qualifiées les solutions qui ne sont pas acides?
d) Citer deux techniques permettant de mesurer le pH.
27) Une effervescence se produit par action de l’acide chlorhydrique sur le zinc.
a) De quel gaz s’agit-il?
b) Par quel méthode peut-on le récupérer?
c) Comment peut-on identifier ce gaz?
28) Je copie et je complète :
Un ion monoatomique est formé à partir ...............................
Un anion monoatomique possède un nombre d’électrons ................ à celui de l’atome correspondant.
La réaction entre le fer et l’acide chlorhydrique produit des ions ............. et du .............. Les ions .......... de l’acide ne réagissent pas.
Une solution qui a un pH de 9 est une solution dite ............ , par exemple, comme ............... ....................... . Par contre, une solution qui a un pH inférieur à 7 est une solution dite ............. , comme la .............. .
29) Quelle est la différence entre un atome et un ion?
30) Comment est constitué un atome?
31) Quelle est la différence entre les deux symboles suivants : Fe et Fe3+ (indiquer la différence du point de vue des charges, lequel est un ion et lequel un atome).
32) Ecrivez les formules des composés suivants :
a) Chlorure de fer III
b) Chlorure de cuivre
c) Sulfate de ferIII
d) Carbonate de sodium
Donnée : ion sulfate : , ion carbonate : , ion sodium Na+ .
33) Un chimiste désire ranger des produits chimiques. Il a trois tubes à essai de solutions qui sont de couleurs différentes : le tube 2 a une couleur verte, le 1 et le 3 sont incolores. Pour savoir ce qu'ils contiennent, il ajoute un peu de soude.
Dans le deuxième, il voit apparaître un précipité vert, dans le premier et le troisième un précipité blanc.
a) Que contiennent les tubes à essai 1,2 et 3?
b) Dans les tubes 1 et 3, il ajoute un excès de soude. Pourquoi? Le précipité disparaît dans le tube 1 et non pas dans le tube 3. Que peut-on conclure?
34) On s’intéresse à la réaction entre le zinc et l’acide chlorhydrique.
a) Quelle est la formule de l’acide chlorhydrique? Expliquez comment caractériser chaque ion.
b) Le zinc et l’acide chlorhydrique réagissent pour former du chlorure de zinc et du dihydrogène.
Quelle est la formule du chlorure de zinc et du dihydrogène?
Comment caractériser la présence de l’ion zinc et du dihydrogène?
c) Ecrire l’équation-bilan en toute lettre puis à l’aide des symboles.
Que doit-on conserver pour équilibrer un réaction chimique?
Equilibrez la réaction.
35) Dilué dans l’eau, l’acide nitrique donne des ions hydroniums et des ions nitrates .
a) Les solutions de cet acide ont-elles un pH inférieur ou supérieur à 7?
b) Donnez leur formule chimique.
c) Cet acide réagit avec le fer. Donnez l’équation-bilan en toute lettre, puis à l’aide des symboles. Pensez à l’équilibrer.
36) Dans une éprouvette, on verse un peu d’acide chlorhydrique dilué sur un fragment de magnésium Mg.
Il se produit une réaction avec un dégagement de dihydrogène et la formation de chlorure de magnésium.
a) Ecrivez la formule du chlorure de magnésium en solution (l’ion magnésium a pour formule Mg2+).
b) Donnez l’équation-bilan de la réaction de l’acide chlorhydrique sur le magnésium.
37) Un chimiste désire ranger des produits chimiques. Il a trois tubes à essai de solutions qui sont de couleurs différentes : le tube 2 a une couleur verte, le 1 et le 3 sont incolores. Pour savoir ce qu'ils contiennent, il ajoute un peu de soude.
Dans le deuxième, il voit apparaître un précipité vert, dans le premier et le troisième un précipité blanc.
a) Que contiennent les tubes à essai 1,2 et 3?
b) Dans les tubes 1 et 3, il ajoute un excès de soude. Pourquoi? Le précipité disparaît dans le tube 1 et non pas dans le tube 3. Que peut-on conclure?
38) Ecrire les équations-bilans des réactions chimiques suivantes (penser à équilibrer) :
1) Le carbone réagit avec le dioxygène pour former du dioxyde de carbone.
2) Le carbone réagit avec le dioxygène pour former du monoxyde de carbone.
3) Le dioxygène et le dihydrogène réagissent pour former de l’eau
4) L’eau donne du dioxygène et le dihydrogène.
5) Le soufre (symbole S) réagit avec le dioxygène pour former du trioxyde de soufre (de symbole SO3).
39)
Donnez la définition dun atome, dune molécule, dun corps simple, et
dun corps composé.
Indiquez
la composition dun atome.
40)
Indiquer parmi les formules suivantes sil sagit datomes ou de molécules
(précisez le nom) :
H2O,
C3H8 (propane), H2, CO2, O, CO, O2.
41)
Indiquez également le nombre total datomes ainsi que la composition de ces
molécules :
H2O,
C3H8, H2, CO2, CO, O2
42)
Indiquez la composition des atomes suivants : Fe , Cl, O, Zn et H.
ZFe=26, ZCl=17,
ZO=8, ZZn=30, ZH=1,
43) Une twingo est recyclable à 90%
a) Citez quelques éléments recyclables.
b) En supposant quelle pèse 603kg, quelle est la masse recyclée ? Que fait-on du reste à votre avis ?
44) Donnez la définition dun atome (niveau 3°, indiquez ce quil y a dans la boule), dune molécule, dun corps simple et dun corps composé.
45) Donnez la composition (nombre total datomes et le nombre de chaque atome) des molécules suivantes :
C6H6
, C2H6O, CO2 , H2O
46) Quest-ce quun ion ? Précisez ce quest un cation et un anion, ainsi que leur composition.
47) Indiquez la composition des atomes suivants : 26Fe, 3Li et 17Cl.
Ces atomes forment parfois les ions suivants : Fe2+, Li+ et Cl-. Indiquez leur composition.
48) Quelle est la composition de latome de carbone 6C et de latome doxygène 8O.
La masse dune charge positive (proton) est de 1,6x10-27 kg et dun électron de 9,11x10-31kg
a) Quel est le plus lourd ?
b) Peut-on négliger la masse de lélectron ? Justifiez.
c) Calculez la masse de latome de carbone et de latome doxygène.
d) On obtient lion O2-. Quelle est sa composition ? Calculez sa masse.
MECANIQUE : 3°
1) Recopiez et complétez le tableau suivant :
Distance 100m ........km 0,8km 1km ........m 80km
Durée 10,2s 20min ........s 1min 40s 8s .....h.....min
Vitesse .......ms-1 90kmh-1 20ms-1 ......kmh-1 120 kmh-1 96 kmh-1
2) Lorsque l'on enfonce une punaise dans un mur, la pointe de la punaise exerce sur le mur une force perpendiculaire à celui-ci, d'intensité 30N.
a) Faites un schéma de la punaise et du mur (le mur sera représenté vertical).
b) Représentez la force à l'échelle après avoir complété un tableau de caractéristique (échelle :1cm <--> 10N).
3) Rappelez la définition d’une force. Par quoi est caractérisée une force? A l'aide de quoi la représente t-on?
4) Vecteurs forces (A est le point d’application)
Direction Horizontale Oblique (45°) Verticale Oblique (30° par rapport à l’horizontale)
Sens Vers la droite Vers le bas à droite Vers le haut Vers le haut à gauche
Valeur 10N 3N 0,02N 2N
Echelle 20N/cm 1,5N/cm 0,005N/cm 0,4N/cm
Représentation
du vecteur-force A. A. A. A.
5) Un automobiliste met 1h22min pour faire 98km.
a) Transformer la durée de parcours en heure.
b) Calculez la vitesse moyenne de l'automobiliste en km.h-1, puis en m.s-1.
6) Combien y a t-il de planètes dans le système solaire? Indiquez-les en commençant par la plus proche du soleil.
7) Un chien a une masse de 5,5kg. Complétez le tableau de caractéristiques du poids. On prendra g=10N/kg.
8) Contravention justifiée?
Un automobiliste parcourt la distance de 85km qui sépare deux postes de péage d’une autoroute en 45 min. Surprise! Deux gendarmes l’attendent à sa sortie pour lui dresser un procès-verbal... « Vous avez dépassé la vitesse limite autorisée » argumentent-ils.
a) Quelle a été la vitesse moyenne de l’automobiliste? Dépasse-t-elle les 130 kmh-1 autorisés?
b) Quelle est alors la raison justifiant l’intervention de la gendarmerie?
9) Un automobiliste met 1h22min pour faire 98km.
a) Transformer la durée de parcours en heure.
b) Calculez la vitesse moyenne de l'automobiliste en km.h-1, puis en m.s-1.
10) Echelles multiples
Echelle (N/m) 5 2 ........ 10 .......
Valeur de la force (N) 35 ....... 16 .......... 9
Longueur du vecteur-force (cm) ....... 2,5 6,4 1,5 4,5
OPTIQUE : 4°
1) Reproduisez le disque réaliser par Newton.
Découpez un cercle de 10cm de diamètre sur une feuille de papier canson. Réalisez 7 secteurs angulaires identiques. Colorez-les des 7 couleurs de l’arc-en-ciel. Puis faites un trou au centre et glissez-y une allumette pour faire une toupie.
Faites-la tourner rapidement : qu’observe t-on?
2) Divers questions!
La terre tourne autour de quel axe?
En combien de temps?
Comment se repère t-on sur le globe?
Quel est notre position?
Pourquoi fait-il jour et nuit?
En combien de temps tourne t-elle autour du soleil?
Que fait-on des 0,25 jours?
La lune est-elle une planète?
En combien de temps tourne t-elle autour de la terre?
La voit-on toujours entière?
Pourquoi?
3) Qu’est-ce qu’une source primaire et une source secondaire de lumière?
Ci-après sont représentées quelques sources de lumières :
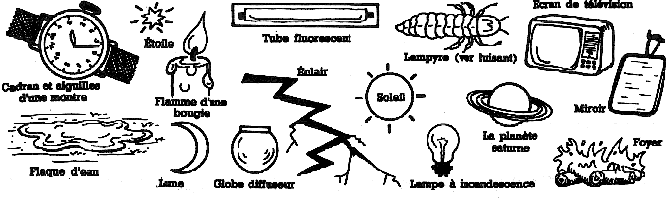
Indiquez les sources qui produisent elles-mêmes de la lumière, les sources qui ne font que renvoyer la lumière qu’elles reçoivent, les sources naturelles de lumière produisant de la lumière par elles-mêmes et les sources artificielles de lumière utilisées pour l’éclairage.
4) Recopiez et complétez :
La lumière blanche est composée de plusieurs ..................... .
La lumière blanche est dite .............................. .
Pour l’arc en ciel, la couleur la plus déviée est le ............, de même pour le .............., alors que pour le .................., c’est le .................... qui est le plus dévié.
5) Comment appelle t-on les 3 couleurs suivantes : le rouge, le bleu et le vert.
6) En certaines circonstances vous avez certainement pu voir un objet très brillant, un avion en général, se déplacer dans le ciel. Pourquoi cet objet était-il aussi lumineux?
7) Le blanc et le noir :
a) Quel est l’effet d’un écran blanc sur la lumière qu’il reçoit? Comment se comporte un écran noir dans les mêmes conditions d’éclairement?
b) Citer des applications pratiques de la peinture blanche, de la peinture noir.
8) Le confort et la mode :
La couleur mode est toujours sombre l’hiver, alors que les collections d’été sont claires et colorées... Quelles sont les explications physiques de ces choix?
9) Pour une renoncule!
La renoncule, appelée aussi bouton-d’or, est une plante toxique mais aux jolies fleurs jaunes. Un jeu d’enfant consiste à placer l’une de ces fleurs sous le menton d’un camarade et à poser la question : « aimes-tu le beurre? »... Quelle que soit la réponse, le résultat est toujours le même!
a) Quelle est la couleur prise par le menton?
Quel est la phénomène physique mis en application dans ce jeu?
10) Vrai ou faux ? Expliquez dans chaque cas votre choix.
a) La couleur d’un objet dépend de la lumière qui l’éclaire.
b) Un objet blanc peut diffuser toutes les lumières, quelle que soit leur couleur.
c) Un objet noir diffuse de la lumière noire.
11) Je choisis la bonne réponse :
a) Eclairé en lumière rouge, un objet rouge paraît .......... (blanc/rouge/noir).
b) Eclairé en lumière bleu, un objet rouge paraît ............ (blanc/rouge/noir).
c) Eclairé en lumière blanche, un objet bleu paraît ............ (blanc/bleu/noir).
12) Recopiez et complétez :
Dans un milieu homogène et transparent, la lumière se propage suivant des ................ appelés ..................... .
La lumière se propage à la vitesse de ...................... km/s ou .................... m/s.
Lors d'une éclipse de Soleil, on ne voit plus ........... ...................... caché par ..... .......................... .
Les saisons sont dues au fait que l'axe qui passe par les pôles est ............. par rapport au plan de ..................... .
13) Indiquer ce que signifie les expressions : zone d'ombre et zone de pénombre.
Faire le schéma d'une éclipse pour expliciter le phénomène.
14) En combien de jours la lune tourne t-elle autour de la Terre?
15) Comment peut-on savoir en regardant la lune si elle est montante ou descendante?
16) La vitesse de propagation de la lumière
a) Quelle est la vitesse de propagation de la lumière en km/s et en km/h?
b) Qu’est-ce qu’une année-lumière (A.L.)? Exprimer une année-lumière en km.
c) Qu’est-ce que l’unité astronomique (U.A.)?
17) La distance moyenne Terre-Lune est de 380000km. Combien de temps la lumière réfléchie par la lune met-elle pour nous parvenir?
18) Combien de temps la lumière émise par le Soleil met-elle à nous parvenir, sachant que la distance moyenne Terre-Soleil est de 150000000km?
19) a) Calculez la vitesse de la lumière en km/h.
b) A quelle distance de la Terre se trouve une planète d’où la lumière met 30 heures pour nous parvenir?
c) Combien de temps (en heures) met la lumière à nous parvenir d’une autre planète située à 1,08x1011km?
20) Notre galaxie comprend 100 milliards d’étoiles environ (estimation).
Combien de temps faudrait-il pour les compter à raison d’une étoile par seconde?
Exprimer en seconde, puis en année.
21) Illusions
-
sur une
feuille, représentez une croix et un point rouge de 0,5cm de diamètre distant
de 10 cm. Fermez lil gauche, avec lil droit, fixez la croix
puis reculez la feuille de lil. Voit-on toujours le point rouge?
- Sur le recto dun carton, de 7 x 4cm, reproduisez un des dessins de la figure ci-dessous. Retournez le carton (haut vers le bas) et reproduisez le deuxième dessin. Adaptez les élastiques dans les trous et faites tourner. Quelle impression a t-on ?
a) La commande à distance dallumage dun téléviseur reste-t-elle efficace lorsquon intercale différents objets entre elle et lecran ?
b)
Réaliser lexpérience en plaçant directement contre la commande les objets
suivants :
-
un livre
-
une règle
-
une
feuille de papier calque
c)
Une commande dallumage émet des rayons infrarouges invisibles. Comment se
comportent ces rayons lorsquils rencontrent des corps opaques ? des
corps transparents ? des corps translucides ?
d)
Placer un livre à une vingtaine de centimètre et actionner la commande.
Que
se passe t-il dans ce cas ?
|
|
|
|
|